Hemos visto en el primer apartado de introducción a la termodinámica química el concepto de sistema y los tipos de sistemas termodinámicos existentes. Ahora bien, una vez delimitado un sistema termodinámico, ¿qué necesitamos conocer para definirlo en profundidad? Necesitamos conocer, además de la composición química del sistema, el valor de una serie de variables que determinan el estado del mismo desde un punto de vista macroscópico. A estas variables se las denomina Variables Termodinámicas. Algunos ejemplos de Variables Termodinámicas son: volumen, temperatura, presión…
Dichas variables se clasifican en dos tipos, atendiendo a su dependencia o independencia con la cantidad total de materia presente en el sistema. Así, tenemos:
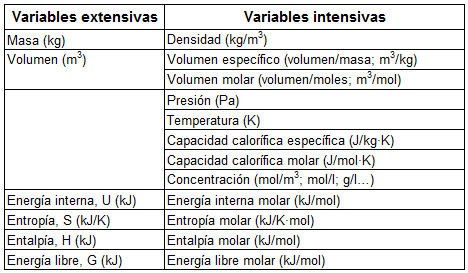
- Variables extensivas: si su valor depende de la cantidad o porción de sistema que se considera, por ejemplo: masa, volumen, número de moles…
- Variables intensivas: si su valor no depende de la cantidad de sistema considerado, por ejemplo: temperatura, densidad, presión, concentración…
Una forma sencilla de distinguir si una variable es extensiva o intensiva es dividir el sistema en dos bloques iguales y considerar si dicha variable cambia o se mantiene constante con respecto al sistema completo. Imaginemos que tenemos el siguiente sistema, constituido por 1 mol de hidrógeno en un recipiente de 22,4 litros:
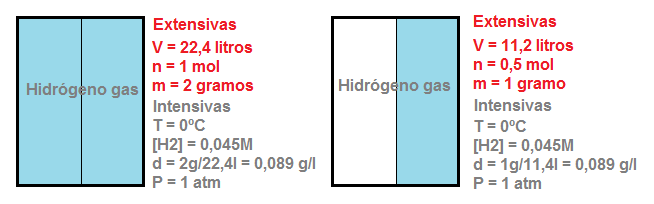
Aunque para el sistema anterior hemos indicado muchas variables, para describir por completo el estado de un sistema no es necesario conocerlas todas, se pueden limitar, dado que las variables termodinámicas se hallan relacionadas entre sí por ecuaciones matemáticas. Por ejemplo, la ecuación de Clapeyron para los gases ideales:
P·V = n·R·T
Donde:
P = presión (atm o pascales, Pa)
V = volumen (litros o m3)
n = número de moles
R = constante de los gases ideales, 0,082 atm·l/K·mol o 8,31 J/K·mol
T = temperatura en grados kelvin (K)
Dada esta ecuación para los gases ideales, bastará conocer la presión, el volumen y la temperatura para definir el estado del sistema, y el número de moles, o la densidad, o la masa, se podrían calcular conociendo dichos valores de P, V y T. Por tanto, con estas variables el sistema quedaría totalmente descrito.
De este modo, un procedimiento habitual a nivel experimental para facilitar el estudio de los sistemas termodinámicos es limitar el número de variables de dicho sistema, manteniendo algunas fijas. Por ejemplo, si estudiamos un proceso a una temperatura constante de 25ºC, la temperatura dejará de ser una variable (no varía) y pasará a ser un valor numérico. Este tipo de proceso en el que se fija una variable adopta su nombre en función de cuál sea la variable fijada:
- A los procesos que se llevan a cabo a temperatura constante, se los denomina isotermos o isotérmicos (T = cte)
- A los procesos que se llevan a cabo a presión constante, se los denomina isobáricos (P = cte)
- A los procesos que se llevan a cabo a volumen constante, se los denomina isocoros (V = cte)
- A los procesos que se llevan a cabo sin transferencia de calor entre el sistema y el entorno, se los llama adiabáticos (Q = 0)
Por último, aunque no por ello menos importante, debemos saber que algunas variables termodinámicas son, además, lo que se conoce como funciones de estado. ¿Qué significa esto? Significa que si el sistema sufre una modificación y pasa de un estado A a un estado B, el valor de estas variables termodinámicas que son funciones de estado no depende de cómo se ha efectuado la transformación, sólo del estado del sistema.
Veremos esto con un ejemplo concreto para que sea más sencillo, tomando como variable la temperatura. Consideremos un sistema que está en un estado A en el cual la temperatura es de 20ºC. Este sistema sufre una transformación y pasa a estar en un estado B en el cual la temperatura es de 60ºC. El sistema en le estado B seguirá estando a 60ºC independientemente del camino que haya seguido la transformación. No depende del camino que ha seguido dicha transformación, no importa si se ha calentado y luego enfriado, o si se ha calentado progresivamente… La temperatura en el estado B seguirá siendo de 60ºC, sin importar cómo se ha llegado a ello. Por esto, la temperatura es una función de estado, sólo depende del estado del sistema en el momento en que lo consideremos.
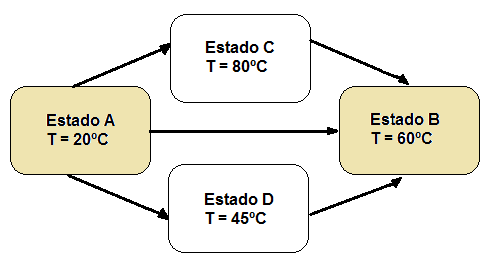
Otra forma de decir esto es que las variaciones que experimentan las funciones de estado sólo dependen del estado inicial y final del sistema. En nuestro caso la variación de temperatura es de 40ºC (60 – 20).
Otras variables termodinámicas que son función de estado son el volumen, la presión, y otros nuevos conceptos en los que vamos a profundizar a lo largo del tema como la energía interna, la entalpía, la entropía y la energía libre de Gibbs.