En este ejercicio de enlace químico nos piden determinar la estructura de Lewis de los iones oxonio, H3O+, y del ion amonio, NH4+, así como indicar la hibridación del átomo central en cada uno de ellos y la geometría esperable.
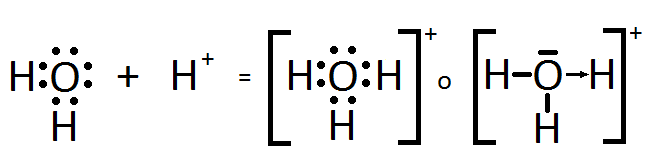
Estructura de Lewis del ión hidronio u oxonio, H3O+
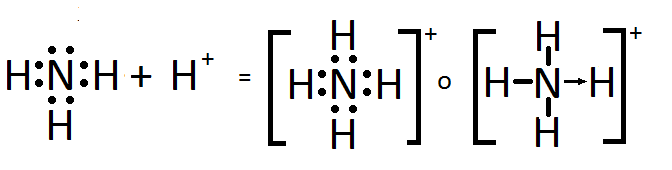
Estructura de Lewis del ión amonio, NH4+
Puesto que ambos iones presentan un átomo central rodeado por 4 pares electrónicos, la disposición de dichos pares será tetraédrica, y la hibridación tanto del oxígeno en el ion oxonio como del nitrógeno en el ion amonio, será hibridación tetraédrica o sp3. No obstante, puesto que el ion oxonio presenta un par de electrones libre, su geometría final no será tetraédrica, ya que el par de electrones no enlazantes no se tiene en cuenta para determinar la geometría. Así, el ión oxonio tendrá geometría de pirámide trigonal, mientras que el ion amonio tendrá geometría tetraédrica (los cuatro pares son enlazantes).
También puede interesarte: